
Старіння здається універсальним біологічним явищем, тим не менше, йому на диво складно дати чітке визначення. За своєю суттю, термін старіння використовують для опису сукупності проявів погіршеного функціонування організму, що корелюють зі збільшенням хронологічного віку людини. Характерні для старіння функціональні зміни, що їх ще називають «біологічними ознаками старіння», відбуваються на молекулярному і клітинному рівнях, знижують фізіологічний гомеостаз та здатність виконувати буремні фізичні та когнітивні задачі. Основна галузь науки що займається старінням людини має назву «геронаука», вона виділяє старіння, як головну причину багатьох хронічних захворювань у пізньому віці, серед яких хвороба Альцгеймера, ішемічна хвороба серця, остеоартрит, інсульт, цукровий діабет 2 типу, а також поширені онкологічні захворювання: рак молочної залози, простати та колоректальний рак. Хоча зниження функціональних можливостей організму характерно для старіння, його темпи дуже різняться. Тоді як деякі люди помирають від хронічних захворювань у віці 60 років, інші все ще залишаються активними і в 100 років.
Коли починається старіння?
Ми чітко знаємо коли старіння закінчується – коли організм помирає. Інша справа, відповісти на питання «коли воно починається?». Загалом існує кілька підходів, і відповідно, декілька варіантів відповіді на дане питання. Дехто вважає, що старіння починається в момент запліднення, інша думка – в момент народження, пубертату, або припинення росту (20 років). Припускають також, що в період найменшої смертності (9 років). Як не дивно, але однієї сталої думки стосовно цього немає навіть серед наукової спільноти даної галузі. Часто говорять, що старіє те, вірогідність смерті чого завтра, більша ніж сьогодні. Логіка зрозуміла, якщо ризик смерті організму збільшується, він старіє, і в старості помирає з більшою ймовірністю. Однак якщо продовжити дивитись на цю залежність в більш ранньому віці, можна припустити, що вона буде зменшуватись, поки не досягне якогось мінімального значення, а цю точку можна буде назвати початком старіння. Однак якщо ми дивимось на цю залежність протягом всього життя, видно, що вона має U подібний вигляд. Таким чином смертність є доволі високою на початку життя, поступово падає, досягає свого мінімуму в 9 років, а далі починає зростати.
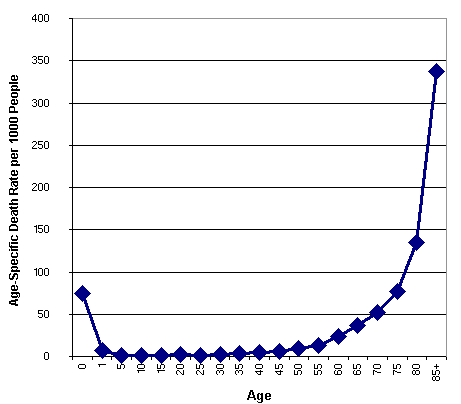
В такому, на перший погляд стрункому підході до визначення процесу старіння є свої проблемні місця. Якщо смертність падає після процесу запліднення в ембріональному періоді, а також до 9 року життя, керуючись даною логіко, чи можемо ми вважати, що організм стає більш молодим? Іншими словами, якщо ми візьмемо двох дітей, 2 та 7 років, котра дитина буде молодшою? Що ж тоді виходить, коли починається старіння? Щоб відповісти на це питання було б добре розуміти, а що є суттю старіння. Для цього треба подивитись на динаміку процесів, що є найважливішими, серед таких є процес накопичення пошкоджень, що є результатом процесу життя. Одними з пошкоджень є мутації, їх залежність не має U подібної форми, їм мало на початку життя і поступово кількість зростає. Другим моментом є епігенетичні зміни. Вони пов’язані з метилюванням нуклеотидів, тут така ж тенденція: спочатку метилювань мало, а далі протягом життя їх кількість зростає. U-подібної залежності також не спостерігається.
Старіння це невідворотній процес чи програма, котру можна перелаштувати?
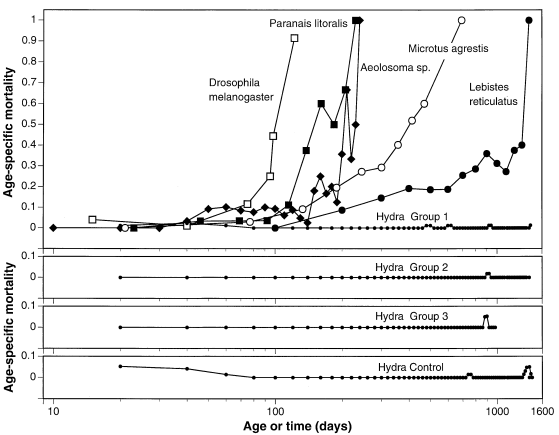
Цікаво, що нам вже відомі організми, що за природніх умов майже не старіють. Вони можуть померти внаслідок різних причин, але з віком вірогідність їх смерті не збільшується. Наприклад, є гідра (Hydra vulgaris), якщо її помістити в середовище зі сприятливими умовами і тривалий час спостерігати за смертністю, то отримаємо графік з прямою горизонтальною лінією. Авжеж вони помирають, однак у цьому випадку ризик смерті не збільшується з віком.

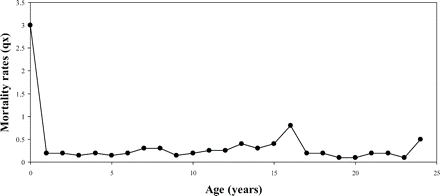
Щодо ссавців, то тут улюбленим об’єктом дослідження геронтологів є голий землекоп (Heterocephalus glaber). Деякі з них, як відомо, прожили більше 30 років, хоча миші та щури, котрі є генетично доволі близькими до голого землекопа живуть 2-3 роки, різниця очевидна.

Чи існує у людей ген довгожителів?
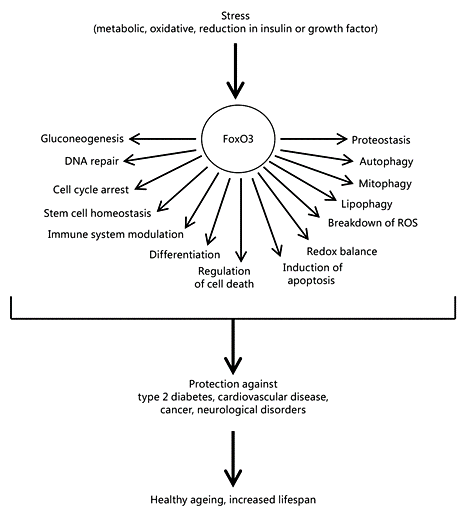
Авжеж, якогось одного абсолютного гену довгожительства немає, однак відомі деякі генетичні варіації, що асоційовані зі збільшеною тривалістю життя. Існує очевидна сімейна схильність до довголіття, котра залежить щонайменше від 300 однонуклеотидних поліморфізмів. Наприклад, серед добре вивчених виділяють ген апопротеїну Е (АпоЕ) та FOXO3А. Останній кодує білок, що є транскрипційним фактором (цей білок зв’язується з ДНК в конкретних місцях, чим активує деякі гени, що розташовані в цих місцях ДНК), відповідно, керує активністю інших генів, серед яких такі, що регулюють клітинну відповідь на стресорні впливи, зокрема шляхом впливу на апоптоз, аутофагію та репарацію ДНК. Відомо, що у разі активації роботи даного гену у деяких тварин (гідра, круглі черви, дрозофіли), тривалість їхнього життя збільшувалась. А здатність FoxO викликати тривалу проліферацію та відновлення стовбурових клітин, а також посилювати імунний нагляд, як вважається, є ключовою причиною безсмертя гідри.
Серед великої кількості механізмів старіння найпопулярнішим (однак не обов’язково найважливішим) є теломерна теорія старіння. Справа в тому, що коли клітина ділиться у неї трішки вкорочуються кінці хромосом, це відбувається через специфіку подвоєння ДНК, що має відбуватись перед кожним поділом клітини. Для того, щоб таке вкорочення кінчиків не зачіпало важливі гени, там є спеціальні кінцеві ділянки – теломери. З кожною реплікацією їх послідовності вкорочуються (див. зображення).
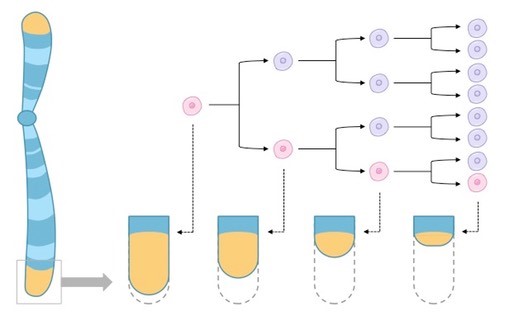
Вважається, що це один з механізмів обмеження кількості поділів соматичних клітин, що лежить в основі всім добре відомого ліміту Гейфліка. Але деякі клітини, котрі в міру своїх функцій мають стрімко і тривало ділитись, мають достатню кількість спеціального ферменту – теломерази, з її допомогою, наприклад, стовбурові клітини можуть відбудовувати ці кінчики хромосом, чим постійно поновлюють здатність клітин до поділу.
Як дізнатись коли прийде смерть: епігенетичний годинник?
Кожна клітина нашого організму має однакову ДНК (геном), але чому одні клітини продукують колаген, інші – інсулін, а деякі взагалі відрощують довжелезні відростки та стають нейронами? Все тому, що різні клітини мають різні епігеноми (різний спосіб пакування ДНК), завдяки цьому одні ділянки ДНК є щільно складеними, а інші – розкритими, що забезпечує легку їх транскрипцію та утворення відповдіних білків, специфічних для конкретної клітини. Таким чином епігеном відповідає за «вмикання» та «вимикання» окремих ділянок ДНК. Це реалізується завдяки білкам гістонам, навколо яких закручується ДНК, а також метилюванню, хімічним сигнальним маркерам, що розміщуються на визначених позиціях ДНК. Отож ідея в тому, що коли організм формується та розвивається епігеном визначає для кожної клітини, яким типом клітин їй бути. Однак коли людина старіє, за однією з гіпотез («epigenetic information theory of aging»), втрачається інформація епігеному. Отож з часом, під дією ушкоджуючих чинників та процесів репарації ДНК гістони не повертаються на своє місце, а метилювання додається в ділянки, де його не мало би бути. Науковці навчились читати ці патерни метилювання та встановлювати з їх допомогою вік людини, і навіть, коли вона найімовірніше помре. Для цього використовується декілька схожих за принципом підходів, один з найпоширеніших має назву «Horvath clock». Загальний принцип полягає в тому, що чим більше метилювання на ДНК в окремих місцях, тим більшим є біологічний вік людини.
Сучасне розуміння механізмів старіння
Оскільки старіння є складним комплексним процесом, для того, щоб можна було виділити механізми, що його забезпечують, вони повинні відповідати наступним вимогам:
1) повинні мати місце за умов нормального старіння;
2) їх експериментальне посилення має прискорювати старіння;
3) експериментальне порушення такого механізму має сповільнювати нормальне старіння, подовжуючи, таким чином, тривалість життя.
Однак слід зазначити, що не для всіх механізмів, про які піде мова далі, дотримані зазначені вимоги. Зокрема, через складність організації експериментальної їх перевірки, особливо 3 пункту.
На молекулярному рівні виділяють наступні стратегії старіння: нестабільність геному (пошкодження ДНК), вкорочення теломер, епігенетичні порушення, втрата білкового гомеостазу. На клітинному рівні старіння асоційоване з виснаженням стовбурових клітин, дисфункцією мітохондрій, що призводить до зменшеного енергоутворення та збільшеного оксидативного стресу, а також порушення міжклітинної комунікації.
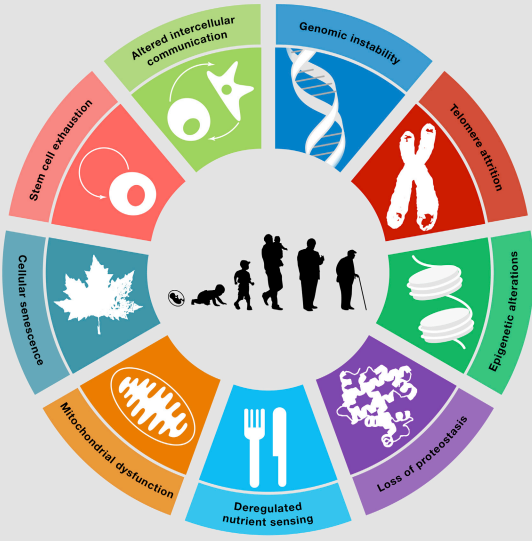
Який виклик стоїть перед людством у боротьбі зі старінням та до чого тут парадокс Пето?
У процесі життя в клітинах нашого організму накопичуються різного роду пошкодження, якісь клітини перестають виконувати свої початкові функції, гірше відновлюються, наростає кількість мутацій в ДНК, одним з наслідків цього може бути ракове переродження таких клітин. Загалом, онкологічні захворювання це вбудований в нас еволюційний процес: клітини мають ділитись, для того, щоб поновлювати ресурс тканин та органів, але оскільки процес ділення клітин не ідеальний, неминуче виникають мутації, котрі рано чи пізно зачіпають гени, відповідальні за контроль поділу клітин. Таким чином, якщо людство зможе подолати всі інші старечі захворювання, а тривалість життя зросте до 200 років, онкологічні захворювання в будь-якому разі, рано чи пізно, дістануть кожного.
Зважаючи на мільярди реакцій та процесів що протікають в нашому організмі кожної миті протягом всього життя питання не втому, чи виникне якийсь збій, питання коли це станеться. Для попередження поганих наслідків таких збоїв, наші клітини мають механізми самознищення (апоптозу). Очевидно, що й вони не ідеальні, тому за наявності достатньої кількості часу, будуть з’являтись клітини з достатньою кількістю порушень, щоб стати раковими. Всі організми мають таку проблему. Але ось що дуже цікаво: клітини всіх організмів мають приблизно однаковий розмір. Іншими словами, клітини миші мають такі ж розміри, як і людські, меншою є лиш їх загальна кількість та тривалість життя. Відповідно, маленька кількість клітин та короткий термін життя зменшують ймовірність того, що щось піде не так. У всякому разі інтуїтивно це здається справедливим. На ділі ж, люди живуть в 50 разів довше ніж миші (2 роки проти 100 років) і мають в 3000 разів більше клітин (10 млрд. проти 30 000 млрд), а ризик розвитку пухлин є приблизно однаковим. Таку ж картину можна побачити порівнюючи людину зі слоном або синім китом. У цьому й полягає парадокс Пето, вирішенням якого займаються науковці різних галузей в надії зрозуміти механізми, що його зумовлюють та розробити на основі цих знань стратегії для подолання серйозної перешкоди на шляху до людського безсмертя – раку.
Громадська організація INgenius – україномовна медична платформа, що пропагує доказову медицину серед спільноти лікарів в Україні з 2016 року. Наша команда створила відкриту базу з перекладених протоколів лікування, аналітичних статей про достовірні методи лікування та розбори фуфломіцинів. Також ми організовуємо на високому рівні події для медиків.
Якщо Ви хочете ще більше доказового україномовного контенту, цікавіших експериментів та практичних заходів, підтримайте нас за допомогою донатів!
Зібрані кошти будуть витрачені на:
- технічне забезпечення сайту;
- щомісячний платіж за платформи такі як ZOOM, telegram і т.д.;
- оплату дизайнера;
- безкоштовні заходи;
- рекламу.
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!

info@ingeniusua.org


