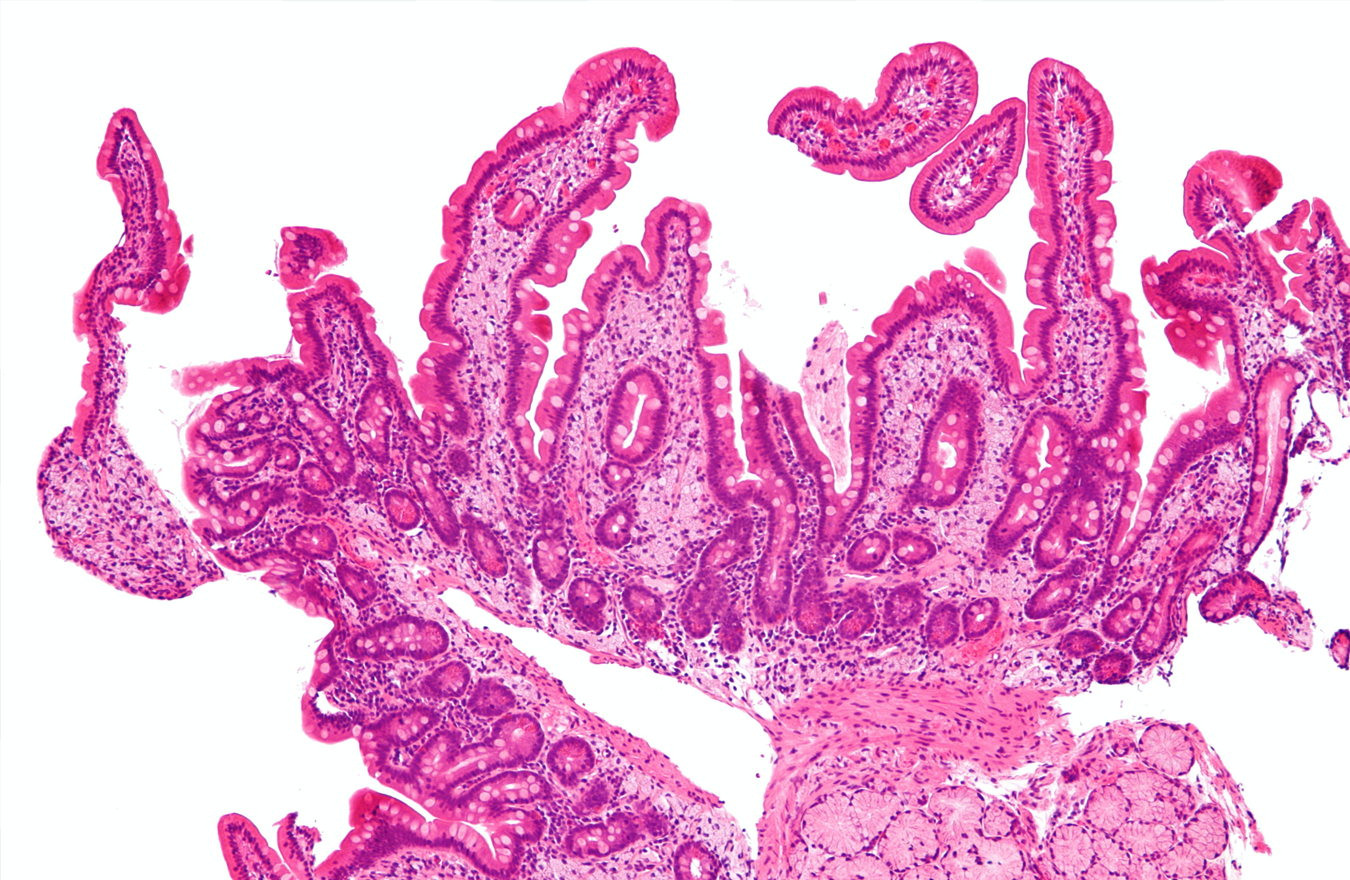
Хвороба Уіппла (Whipple disease) — це рідкісне хронічне інфекційне захворювання. В популяції зустрічається з частотою 1/1 000 000, хоча останнім часом його почали виявляти значно частіше, ймовірно, завдяки удосконаленню діагностичних стратегій. Хворіють переважно чоловіки у віці 40-60 років.
Збудником хвороби Уіппла є троферима Уіппла (Tropheryma whipplei) — грам-позитивна актинобактерія, вперше описана ще в 1907 році англійський вченим Джорджем Уіпплом. Під час проведення аутопсії пацієнта, що страждав тривалою діареєю, гарячкою та значною втратою ваги, Уіппл знайшов “сріблясті паличкоподібні бактерії” всередині макрофагів в тонкому кишечнику. Щоправда, тоді він не пов’язав свою знахідку із безпосереднім розвитком захворювання і майже до кінця ХХ століття хвороба Уіппла вважалася формою ліподистрофії тонкого кишечника виключно аутоімунного походження. Тут варто наголосити, що хоч бактерія T. whipplei безсумнівно є безпосереднім збудником хвороби Уіппла, для розвитку захворювання необхідний ще цілий ряд чинників, серед яких і генетична схильність.
Існує 3 основні клінічні форми захворювання:
1. Класична (80% випадків). Ділиться на продромальну та прогресуючу фази.
Продромальна фаза триває в середньому 6-8 років і для неї характерні абсолютно неспецифічні симптоми, такі як артралгії/артрити, гарячка, загальна слабкість, лімфаденопатія. Серед лабораторних показників часто спостерігають підвищення рівню С-реактивного білку, ШОЕ, лейкоцитоз і тромбоцитоз. Така картина наштовхує більшість клініцистів на ідею ревматологічної патології із подальшим призначенням імуносупресивної терапії, що в переважній більшості випадків суттєво погіршує перебіг захворювання (особливо якщо йдеться про антагоністи TNF-α рецепторів).
Фаза прогресування характеризується появою симптомів мальабсорбції: втратою ваги, діареєю/стеатореєю (часто супроводжується болем в животі), а також дефіцитними синдромами (анемія, гіпоальбумінемія тощо). Крім того, досить часто розвиваються гепато- та спленомегалія, інколи асцит. Не рідкістю є ураження нирок та шкіри.
2. Асоційована з ендокардитом. В більшості таких пацієнтів немає ознак класичної форми хвороби Уіппла і присутні лише кардіологічні симптоми. На відміну від більшості інших збудників ендокардиту, у випадку T. whipplei мова йде про внутрішньоклітинну інфекцію, а тому в крові культура цих бактерій не визначається. Оскільки специфічних діагностичних критеріїв немає, то є сенс запідозрити асоційований з T. whipplei ендокардит як діагноз-виключення у чоловіків європеоїдів віком 45-60 років, що маєть великі вегетації та негативну гемокультуру.
3. Ізольована неврологічна форма. Зустрічається вкрай рідко, характеризується гетерогенними симптомами, серед яких є головні болі, судоми, порушення сну, когнітивні та окорухові розлади. Патогномонічним симптомом вважається окуломастикаторна міоритмія.
Діагностика
Основним методом є проведення ендоскопії з дослідженням біоптатів з уражених ділянок проксимального відділу тонкої кишки у хворих з класичною формою захворювання. У випадку більш рідкісних форм можна досліджувати вегетації серцевих клапанів, спинномозкову рідину.
Крок 1. Гістологічне дослідження біоптату з використанням:
- ШИК-реакції (вона ж Periodic acid Schiff reaction), внаслідок якої бактерії набувають малиново-фіолетового забарвлення. Є досить чутливою, але не надто специфічною для цього збудника.
- Фарбування за Цілем-Нільсеном можна використати для диференційної діагностики з мікобактеріями (T. whipplei буде синього забарвлення як не кислотостійка).
Крок 2. Проведення ПЛР для безпосереднього виявлення ДНК збудника.
Захворювання при відсутності вчасно розпочатого лікування може бути летальним.
Лікування
Етіотропне лікування потребує призначення антибіотиків. Зараз не існує єдиного стандартизованого протоколу лікування.
Зокрема, в Німеччині найпоширенішим є двотижневий курс, що включає парентеральне введення цефтріаксону або меропенему, після якого йде підтримуюча терапія триметопримом/сульфаметоксазолом (котримоксазол) протягом 1 року (на сьогодні існують дані, згідно яких є сенс скоротити підтримуючу терапію до 3 місяців).
Альтернативна схема передбачає застосування комбінації з доксицикліном та гідроксихлорохіном протягом 1 року із подальшим пожиттєвим прийомом доксацикліну.
Оскільки ризик розвитку рецидиву захворювання досить високий, дуже важливу роль відіграє подальше спостереження, яке включає клінічне, лабораторне та інструментальне обстеження на 6, 12, 24 та 36 місяцях після встановлення діагнозу. Надалі — контрольні огляди кожні 3 роки.
Автор зображення: Michael Bonert
Статтю підготувала: Діана Жегестовська
Громадська організація INgenius – україномовна медична платформа, що пропагує доказову медицину серед спільноти лікарів в Україні з 2016 року. Наша команда створила відкриту базу з перекладених протоколів лікування, аналітичних статей про достовірні методи лікування та розбори фуфломіцинів. Також ми організовуємо на високому рівні події для медиків.
Якщо Ви хочете ще більше доказового україномовного контенту, цікавіших експериментів та практичних заходів, підтримайте нас за допомогою донатів!
Зібрані кошти будуть витрачені на:
- технічне забезпечення сайту;
- щомісячний платіж за платформи такі як ZOOM, telegram і т.д.;
- оплату дизайнера;
- безкоштовні заходи;
- рекламу.
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!

info@ingeniusua.org