
Наші знання про структуру та функцію мРНК розширилися від уявлення про неї як про просто проміжну молекулу між ДНК та білками, до усвідомлення того, що РНК є динамічним генним регулятором, який можна модифікувати та редагувати. Так дана структура стала предметом інтересу для розробки нових терапевтичних схем проти певних інфекційних, нейродегенеративних, а останнім часом і серцево-судинних захворюваннь. Сьогодні antisense oligonucleotides (ASO), small interfering RNAs (siRNAs) та microRNAs (зберігаємо оригінальні назви, заради запобігання термінологічних непорозумінь) є одними з найбільш широко застосовуваними терапевтичними стратегіями цільового регулювання експресії генів та синтезу білків. Однак необхідно подолати ряд бар'єрів, включаючи нестабільність, неадекватну спорідненість до зв'язування та доставку в тканини, імуногенність та небажану токсичність, для того, щоб ці агенти перетворилися на ефективні ліки. Оскільки серцево-судинні захворювання залишаються головною причиною смертності у всьому світі, значне число клінічних випробувань проводиться саме з метою вивчення безпеки та ефективності РНК-терапії в таких клінічних станах як сімейна гіперхолестеринемія, цукровий діабет, гіпертригліцеридемія, серцевий амілоїдоз та фібриляція передсердь. То які ж таргети подібного лікування існують на сьогоднішній день?
1.Аполіпопротеїн В (ApoB), є важливим структурним компонентом усіх атерогенних ліпопротеїдів, включаючи холестерин ліпопротеїдів низької щільності (LDL-C), відповідальний за транспорт і виведення LDL-C, та є фактором ризику виникнення серцево-судинних захворювань. Mipomersen — це 20-нуклеотидний антисмисловий олігонуклеотид, націлений на мРНК ApoB, механізм дії якого полягає у зв’язуванні з рибонуклеїновою кислотою ApoB та інгібуванні подальшого синтезу білка.
2. Схвалення Mipomersen FDA відкрило шлях до дослідження інших можливих таргетів з використанням антисмислової технології в області серцево-судинних захворювань. Однією з найбільш перспективних мішеней є PCSK9 (proprotein convertase subtilisin/kexin-9), який у нормі відповідає за знижену експресію рецепторів для ЛПНЩ на поверхні клітин печінки, а значить і знижений транспорт ЛПНЩ у гепатоцити, що призводить до підвищеного їх рівня у крові. Окрім терапевтичних засобів, що функціонуватимуть на основі механізмів дії, описаних вище, та досі досліджуються, FDA нещодавно схвалила два препарати моноклональних антитіл проти PCSK9 — Evolocumab таAlirocumab.
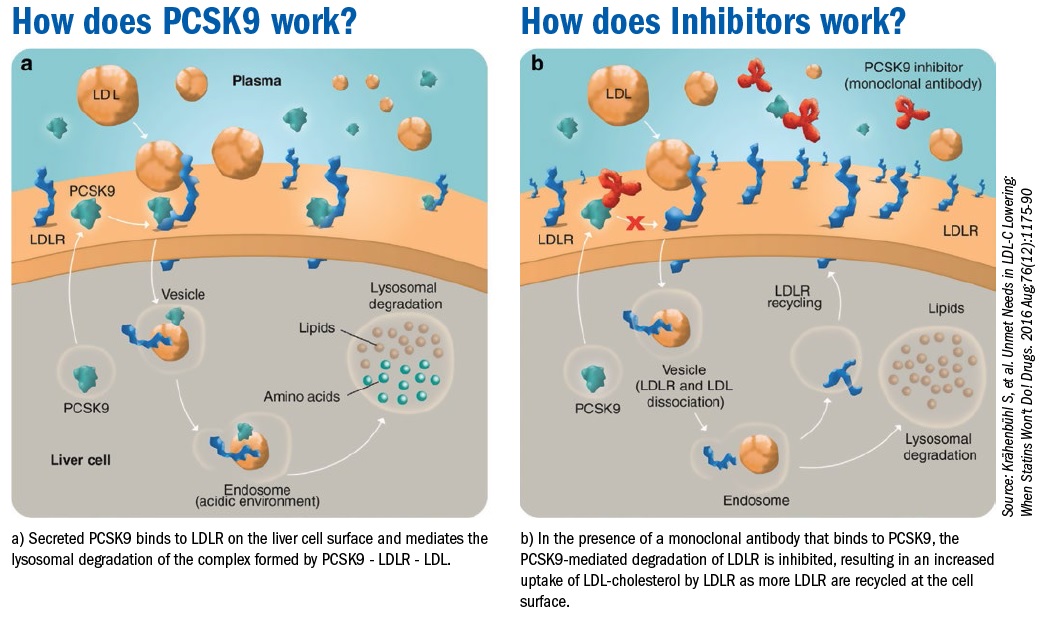
Лікування інгібіторами PCSK9, Evolocumab and Alirocumab, знижує рівень ЛПНЩ на ~ 60% (Desai et al., 2017). Цікаво, що дослідження FOURIER (Further Cardiovascular Outcomes Research With PCSK9 Inhibition in Subjects With Elevated Risk) показало додаткову користь для серцево-судинної системи, яке здійснює інгібування PCSK9, крім ефекту зниження рівнів ліпідів. Так, Evolocumab значно знизив ризик серцево-судинної смерті, інфаркту міокарда, інсульту, госпіталізації з приводу нестабільної стенокардії або коронарної реваскуляризації на 15% порівняно з контрольною групою пацієнтів (Sabatine et al., 2017).
3. Аполіпопротеїн С3 (APOC-III) — ще один можливий таргет у пацієнтів, що страждають сімейною хіломікронемією. APOC-III проявляє свою атерогенну дію, послаблюючи ліполіз багатих тригліцеридами ліпопротеїнів за допомогою інгібування ліпопротеїд-ліпази, що призводить до підвищення рівня циркуляції ліпопротеїдів і хіломікронів дуже низької щільності у крові. Підвищений рівень APOC-III реєструється у пацієнтів з гіпертригліцеридемією та є причинно пов'язаним з метаболічним синдромом та резистентністю до інсуліну (Baldi et al., 2013). Носії ж мутацій, що порушують функцію APOC-III, мають на 40% нижчий ризик розвитку ішемічної хвороби серця порівняно з неносіями (TG and HDL Working Group of the Exome Sequencing Project et al., 2014). На сьогоднішній день розроблений Volanesorsen, антисмисловий олігонуклеотид другого покоління, який був націлений на мРНК APOC-III і подає надії для лікування пацієнтів із сімейним синдромом хіломікронемії. Прогнозоване закінчення його клінічного дослідження припадає на 2021 рік.
Громадська організація INgenius – україномовна медична платформа, що пропагує доказову медицину серед спільноти лікарів в Україні з 2016 року. Наша команда створила відкриту базу з перекладених протоколів лікування, аналітичних статей про достовірні методи лікування та розбори фуфломіцинів. Також ми організовуємо на високому рівні події для медиків.
Якщо Ви хочете ще більше доказового україномовного контенту, цікавіших експериментів та практичних заходів, підтримайте нас за допомогою донатів!
Зібрані кошти будуть витрачені на:
- технічне забезпечення сайту;
- щомісячний платіж за платформи такі як ZOOM, telegram і т.д.;
- оплату дизайнера;
- безкоштовні заходи;
- рекламу.
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!

info@ingeniusua.org


