
Часто пацієнти з ГКМП залишаються безсимптомними або злегка симптоматичними і звертаються до лікаря після виявлення внушаючого сімейного анамнезу, виявлення шумів при фізикальному обстеженні або аномальної електрокардіограми (ЕКГ). Найбільш часто зустрічаються симптоми — задишка, втома, дискомфорт у грудях, прискорене серцебиття, пресінкопе і непритомність. Важливі історичні підказки включають прогресивну непереносимість фізичного навантаження чи непритомність під час або відразу після фізичного навантаження або при зневодненні.
Сімейний анамнез покоління повинен бути виявлений при первинній оцінці, орієнтуючись на родичів з будь-якими серцевими діагнозами, «товстими» серцями, «серцевим нападом» або інсультом на початку життя, аномальними серцевими ритмами, постійними кардіостимуляторами або імплантованими дефібриляторами серця, серцевою недостатністю або трансплантацією серця. Історія раптової смерті повинна викликати цілеспрямовані питання щодо родичів з передчасною або несподіваною смертю, смерті, пов'язаної з фізичним навантаженням, і доступності аутопсії або посмертного генетичного тестування.
При фізикальному огляді наявність різкого «зростаючого – зменшуючого» систолічного шуму на нижній лівій стернальній границі, середньо-пізній систолічний апікальний шум або голососистолічний апікальний шум і / або парадоксально розділений S2 повинні попередити клініцистів про можливість ГКМП.
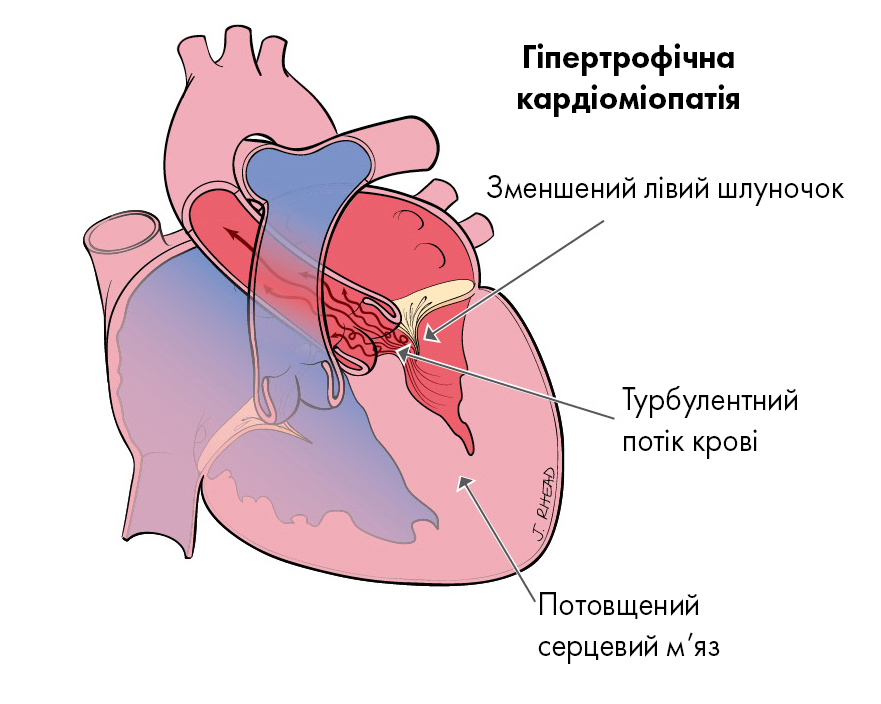
Постановка діагнозу
Діагноз ГКМП підтверджується наявністю товщини стінки лівого шлуночка ≥15 мм, яка в іншому випадку не може бути пояснена ненормальними умовами навантаження (наприклад, гіпертонією, клапанними, вродженими захворюваннями) або інфільтративними кардіоміопатіями. Незрозумілою товщиною стінки лівого шлуночка ≥13 мм достатньо для діагностики у родичів осіб з ГКМП або тих, хто має позитивний генотип. Базальна перегородка є найбільш поширеним місцем для гіпертрофії, також спостерігаються множинні інші моделі асиметричної гіпертрофії (кривизна перегородки перегину, сигмовидна перегородка, нейтральна перегородка, середина шлуночка, апікальна).
Наявність, розташування і механізм обструкції лівого шлуночка слід ідентифікувати за допомогою послідовного доплерівського безперервного моніторування від вершини лівого шлуночка до основи з обережністю, щоб уникнути перехресного забруднення градієнта відтоку лівого шлуночка і сигналів мітральної регургітації. Градієнт відтоку лівого шлуночка слід вимірювати в спокої. Якщо максимальний миттєвий доплеровській градієнт безперервної хвилі становить 50 мм рт.ст., то провокаційні заходи, включаючи маневр Вальсальви під час ехокардіографії в спокої або вправи під час стрес-ехокардіографії на біговій доріжці, можуть викликати градієнт. Піковий миттєвий доплеровській градієнт безперервної хвилі ≥30 мм рт. в стані спокою вказує на обструктивну фізіологію, а градієнт ≥50 мм рт.ст. в спокої або з провокацією вважається порогом для відновлення перегородки у пацієнтів з симптомами.
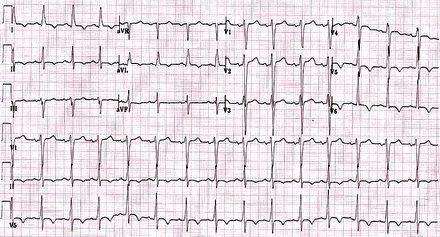
Беручи до уваги, що відхилення, які спостерігаються на ЕКГ з 12 відведеннями, не є специфічними для ГКМП, такі результати, як локалізовані або широко поширені зміни реполяризації (включаючи інверсію зубця Т), помітні прекардіальні напруження і відхилення лівої осі (що наводять на думку про гіпертрофію шлуночка), відхилення зубця Р (наводить на думку про розширення лівого передсердя), і нижні і / або бічні зубці Q (наводить на думку про гіпертрофовану септальну деполяризацію) повинні викликати підозри на розлад.
Магнітно-резонансна томографія серця (МРТ) забезпечує чудові морфологічні і тканинні характеристики і об'ємну оцінку в порівнянні з ехокардіографією. МРТ серця рекомендується:
1) пацієнтам, у яких ехокардіографія не дозволяє встановити діагноз ГКМП
2) пацієнти з відомим ГКМП, для яких додаткова інформація, що стосується величини і розподілу гіпертрофії або анатомії апарату мітрального клапана, була б корисна при прийнятті рішення щодо терапії для зменшення перегородки.
Великі проспективні дослідження щодо прогностичної користі МРТ з контрастним посиленням при стратифікації ризику раптової смерті тривають.
Диференційна діагностика
Системна гіпертензія і стеноз аорти є найбільш поширеними причинами набутої гіпертрофії лівого шлуночка і повинні бути виключені при підозрі на ГКМП. Фізіологічне ремоделювання у зв'язку з фізичною підготовкою може також проявлятися потовщенням стінки лівого шлуночка, але зазвичай його можна відрізнити від ГКМП, використовуючи комбінацію візуалізації і функціонального тестування. При фізіологічному ремоделюванні товщина стінки лівого шлуночка рідко перевищує 15 мм, а розміри порожнини лівого шлуночка, як правило, більші у порівнянні з типовими розмірами лівого шлуночка в ГКМП. Діастолічна функція, включаючи тканинні допплерівські вимірювання, повинна бути нормальною в випадках фізіологічного ремоделювання.
Генетично опосередковані фенокопії ГКМП (наприклад, хвороба Андерсона-Фабрі [GLA], хвороба Данона [LAMP2], хвороба Помпе [GAA], AMPK-опосередкована хвороба накопичення глікогену [PRKAG2], амілоїдоз [TTR], атаксія Фрідрейха [FRDA]), міотонічна дисторфія [DMPK, ZNF9]) слід враховувати при первинній оцінці гіпертрофії лівого шлуночка. Патерни успадкування, поліорганного (особливо неврологічного, скелетно-м'язового, ниркового) ураження і характеристики ЕКГ, такі як попереднє порушення, корисні для диференціації ГКМП від цих розладів.
Генетичне тестування і скринінг
Пацієнти, які проходять генетичне тестування, повинні також проходити консультування когось, хто знає про генетику серцево-судинних захворювань, щоб результати і їх клінічне значення могли бути відповідним чином розглянуті з пацієнтом. Хоча генетичне тестування не потрібно для діагностики ГКМП, тестування на причинно-наслідкові / пов'язані із захворюванням генетичні варіанти слід пропонувати пробанду, якщо є нетиповий прояв або коли підозрюється інше генетичне захворювання. У сучасній практиці комерційні компанії по генетичному тестуванню зазвичай пропонують цільове генетичне секвенування 50-100 генів, пов'язаних з кардіоміопатією.
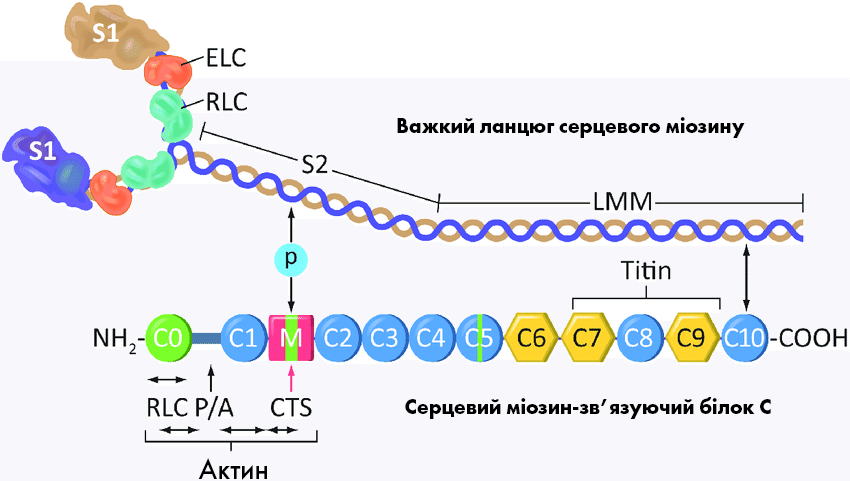
Генетичне тестування також доцільно, щоб полегшити виявлення членів сім'ї першого ступеня, схильних до ризику розвитку ГКМП. Якщо у пробанда і постраждалих родичів виявлена генетична причина виникнення ГКМП, родичі, у яких немає сімейного варіанту, можуть бути виключені з поточного клінічного скринінгу. Якщо генетичне тестування не проводиться або причинний варіант не виявлено в пробанда, рекомендується постійне періодичне клінічне спостереження за родичами за допомогою електрокардіографії та ехокардіографії кожні 3-5 років.
Пацієнти з ГКМП мають широкий спектр проявів: від безсимптомних з внушаючим сімейним анамнезом, шумом, ненормальною ЕКГ або ехокардіограмою до симптомів серцевої недостатності, від обструкції відтоку або обмежувальної фізіології до раптової серцевої смерті. Ехокардіографія є ключем до діагностики, і МРТ може зіграти майбутню роль в стратифікації ризику раптової смерті. Оцінка генетично опосередкованих фенокопій або фізіологічного ремоделювання є важливою, тому що ці діагнози можуть змінити лікування. У міру того, як зростає розуміння генетичної основи ГКМП, генетичне тестування може запропонувати більш глибоке розуміння і має завжди відбуватися в поєднанні з генетичним консультуванням, щоб пацієнти і члени сім'ї могли найкраще оцінити наслідки отриманих результатів.
Громадська організація INgenius – україномовна медична платформа, що пропагує доказову медицину серед спільноти лікарів в Україні з 2016 року. Наша команда створила відкриту базу з перекладених протоколів лікування, аналітичних статей про достовірні методи лікування та розбори фуфломіцинів. Також ми організовуємо на високому рівні події для медиків.
Якщо Ви хочете ще більше доказового україномовного контенту, цікавіших експериментів та практичних заходів, підтримайте нас за допомогою донатів!
Зібрані кошти будуть витрачені на:
- технічне забезпечення сайту;
- щомісячний платіж за платформи такі як ZOOM, telegram і т.д.;
- оплату дизайнера;
- безкоштовні заходи;
- рекламу.
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!
Кожний Ваш внесок - це вклад у майбутнє не тільки наше як платформи, але й також у прогресивний розвиток доказової медицини в України.
Revolution in you!

info@ingeniusua.org